टाइप 2 न्यूरोफाइब्रोमैटोसिस के लिए दवा। टाइप II न्यूरोफाइब्रोमैटोसिस के न्यूरोसर्जिकल पहलू
टाइप 2 न्यूरोफाइब्रोमैटोसिस (एनएफ२) 1:33000 से 1:50,000 की घटनाओं के साथ NF1 न्यूरोफाइब्रोमैटोसिस की तुलना में बहुत कम आम है। NF2 को एक ऑटोसोमल प्रमुख तरीके से विरासत में मिला है, जिसमें जीन पैठ 95% से अधिक है। NF2 अक्सर जीवन के दूसरे और तीसरे दशक में खुद को प्रकट करता है। कैंटर एट अल के अनुसार, वेस्टिबुलर श्वानोमा के लक्षणों की शुरुआत में औसत आयु 20.4 वर्ष है।
पर वेस्टिबुलर श्वानोमासलगभग 8% इंट्राक्रैनील ट्यूमर और लगभग 80% कोणीय सेरेबेलोपोंटिन ट्यूमर के लिए जिम्मेदार हैं। अधिकांश वेस्टिबुलर श्वानोमा छिटपुट और एकतरफा होते हैं, जो पांचवें दशक में प्रकट होते हैं।
रोगियों के साथ न्यूरोफाइब्रोमैटोसिस टाइप 2(NF2) और द्विपक्षीय वेस्टिबुलर श्वानोमास वेस्टिबुलर श्वानोमास के सभी मामलों में 2 से 4% के लिए खाते हैं।
टाइप 2 न्यूरोफाइब्रोमैटोसिसअक्सर NF1 के साथ भ्रमित होता है। अंतिम प्रमाण कि NF1 और NF2 अलग-अलग इकाइयाँ हैं, 1987 तक संभव नहीं था। बार्कर एट अल द्वारा किए गए आणविक जैविक अध्ययनों सहित कई अध्ययनों से पता चला है कि NF1 के विकास के लिए जिम्मेदार जीन गुणसूत्र 17 की लंबी भुजा के समीपस्थ छोर के पास स्थानीयकृत है। रूएलाउ एट अल द्वारा इसी अवधि के दौरान किया गया एक स्वतंत्र अध्ययन। ने दिखाया कि NF2 के लिए जिम्मेदार जीन गुणसूत्र 22 पर स्थानीयकृत है।
टाइप 2 न्यूरोफाइब्रोमैटोसिसगुणसूत्र 22 पर स्थित जीन उत्परिवर्तन के वंशानुक्रम के परिणामस्वरूप विकसित होता है। जीन के भीतर उत्परिवर्तन की आवृत्ति 6.5 x 10 -6 होने का अनुमान है। इन रोगियों में, लगभग 50% मामलों में, कोई पारिवारिक इतिहास नहीं होता है और नए जनन उत्परिवर्तन होते हैं। यह गुणसूत्र 22 था जो 1982 में मेनिंगियोमा के साइटोजेनेटिक अध्ययन के बाद एनएफ 2 के संभावित स्रोत के रूप में सामने आया था। एचएफ 2 जीन को बाद में 1986 और 1987 में क्रमशः लिंकेज और हेटेरोज़ायोसिटी विश्लेषण दोनों के डेटा के आधार पर गुणसूत्र 22 को सौंपा गया था।
में १९९३ वर्षशोधकर्ताओं के दो स्वतंत्र समूहों ने एनएफ 2 जीन को अलग कर दिया है, जिसे मर्लिन या स्च्वानोमाइन कहा जाता है। HF2 जीन गुणसूत्र 22q12.2 पर 100 kb से अधिक तक फैला हुआ है और इसमें 17 एक्सॉन हैं। मैसेंजर आरएनए कोडिंग अनुक्रम 1785 बीपी लंबाई में है और 595 एमिनो एसिड प्रोटीन को एन्कोड करता है। जीन उत्पाद प्रोटीन के परिवार के करीब है, जिसमें मोसिन, एज़्रिन, रेडिक्सिन, टैलिन और अन्य शामिल हैं जो 4.1 प्रोटीन सबफ़ैमिली का हिस्सा हैं। ये प्रोटीन साइटोस्केलेटन घटकों के साइटोप्लाज्मिक झिल्ली के आसंजन में शामिल होते हैं और एक्टिन-समृद्ध माइक्रोविली में स्थानीयकृत होते हैं। यह माना जाता है कि मर्लिन प्रोटीन का एन-टर्मिनल क्षेत्र साइटोप्लाज्मिक झिल्ली के घटकों के साथ इंटरैक्ट करता है, और सी-टर्मिनल क्षेत्र साइटोस्केलेटन के साथ इंटरैक्ट करता है।
मर्लिन या श्वानोमाइन मुख्य रूप से व्यक्त किया जाता है तंत्रिका तंत्र की कोशिकाओं और लेंस में... वर्तमान में यह माना जाता है कि मर्लिन प्रोटीन की अधिकता कोशिका वृद्धि को रोक सकती है और यह कोशिका की सतह और कोशिका बढ़ाव पर प्रोट्रूशियंस के निर्माण में योगदान देता है। 1994 में, टिकू एट अल। एक ट्यूमर जीन शमनकर्ता के रूप में मर्लिन की क्षमता का परीक्षण किया। इसके बाद, v-Ha-Ras-रूपांतरित NIH 3T3 कोशिकाओं में NF2 प्रोटीन पेश करके, वे घातक फेनोटाइप के उन्मूलन को प्रदर्शित करने में सक्षम थे, और इस प्रकार ट्यूमर को दबाने के लिए मर्लिन की क्षमता की पुष्टि करते हैं।
हालांकि सटीक NF2 प्रोटीन कार्यपूरी तरह से समझा नहीं गया है, उपलब्ध डेटा इंगित करता है कि यह इंटरसेलुलर या सेल-मेम्ब्रेन इंटरैक्शन में शामिल है और सेल की गति, आकार और बातचीत में महत्वपूर्ण भूमिका निभाता है। प्रोटीन मर्लिन के कार्यों के नुकसान के परिणामस्वरूप, संपर्क अवरोध का उल्लंघन देखा जा सकता है, जिससे ऑन्कोजेनेसिस होता है।
उत्परिवर्तन शामिल जीन NF2, छिटपुट वेस्टिबुलर श्वानोमा वाले 22-59% रोगियों में देखे जाते हैं। वेलिंग एट अल। छिटपुट वेस्टिबुलर श्वानोमा वाले रोगियों में और NF2 के रोगियों में आनुवंशिक उत्परिवर्तन का पता लगाने की आवृत्ति की तुलना की और क्रमशः 66 और 33% का महत्वपूर्ण अंतर पाया, यह देखते हुए कि ऑन्कोजेनेसिस में विभिन्न उत्परिवर्तन तंत्र हो सकते हैं। आज तक, NF2 जीन के 200 से अधिक उत्परिवर्तन की पहचान की गई है, जिसमें एकल आधार प्रतिस्थापन, सम्मिलन और विलोपन शामिल हैं। अधिकांश उत्परिवर्तन प्रोटीन के सी-टर्मिनल सिरे को काट देते हैं; मिसेज़ म्यूटेशन में से केवल 13 की पहचान की गई है।
दोष के जीन NF2मेनिंगिओमास, घातक मेसोथेलियोमास, मेलानोमा और स्तन कैंसर सहित अन्य नियोप्लाज्म में पाया जाता है।
अध्ययन जीनोटाइप-फेनोटाइप सहसंबंधपता चलता है कि NF2 जीन में उत्परिवर्तन विभिन्न फेनोटाइपिक अभिव्यक्ति से जुड़े हैं। रटलेज एट अल। पाया गया कि प्रोटीन कतरन के परिणामस्वरूप एचएफ 2 जीन में उत्परिवर्तन एचएफ 2 (विशार्ट) के अधिक गंभीर नैदानिक अभिव्यक्तियों से जुड़ा हुआ है, जबकि मिसेन्स और स्प्लिस साइट म्यूटेशन हल्के रोग प्रगति (गार्डनर) से जुड़े हैं।
बचावऔर अन्य। यह भी संकेत दिया कि रेटिना के घाव अधिक विनाशकारी जीन प्रोटीन क्लिपिंग म्यूटेशन से जुड़े हैं। दोनों अध्ययनों में फेनोटाइपिक अभिव्यक्ति में इंट्राफैमिलियल अंतर पाया गया।
हालांकि NF2 जीन का उत्परिवर्तनवेस्टिबुलर श्वानोमास की प्रकृति में एक प्रमुख भूमिका निभाते हैं, यह संभव है कि अन्य आनुवंशिक लोकी वेस्टिबुलर श्वानोमास के विकास में योगदान करते हैं। उपरोक्त के अलावा, यह ध्यान दिया जाना चाहिए कि न्यूरोफाइब्रोमैटोसिस टाइप 2 (एनएफ 2) के लिए जीन के उत्परिवर्तन वेस्टिबुलर श्वानोमा वाले सभी रोगियों में पाए जाते हैं, जबकि जीनोटाइपिक-फेनोटाइपिक सहसंबंध संभव हैं, जिसके अस्तित्व से पता चलता है कि अन्य आनुवंशिक लोकी भी हो सकते हैं। वेस्टिबुलर श्वानोमास की घटना और रोगियों के अंतिम फेनोटाइप में योगदान करते हैं।
जीन का पता लगाना, NF2 . के लिए जिम्मेदारमोटे तौर पर आणविक स्तर पर विकृति विज्ञान की हमारी समझ और न्यूरोफाइब्रोमैटोसिस टाइप 2 (एनएफ 2) वाले रोगियों में नैदानिक विषमता के लिए जिम्मेदार कारकों पर निर्भर करता है। जल्द ही, ट्यूमर के गठन में मर्लिन के कार्यों को समझना एंटीट्यूमर थेरेपी के विकास का आधार बन जाएगा, जो अंततः न्यूरोफाइब्रोमैटोसिस टाइप 2 (एनएफ 2) से जुड़े रोगियों की पीड़ा को कम कर सकता है।
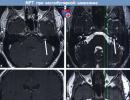
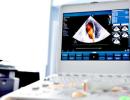
 कंट्रास्ट एन्हांसमेंट के साथ एमपीटी, टी1 मोड।
कंट्रास्ट एन्हांसमेंट के साथ एमपीटी, टी1 मोड। (ए) अक्षीय और (सी) ललाट वर्गों में बाईं ओर इंट्राकैनालिक्युलर वेस्टिबुलर श्वानोमा (वीएस, तीर)।
वेस्टिबुलर श्वानोमा (वीएस) उस क्षेत्र में स्थित है जहां आंतरिक श्रवण नहर के क्षेत्र में मस्तिष्कमेरु द्रव (तीर) से कोई संकेत नहीं है (बी) सीआईएसएस अनुक्रम में उच्च-रिज़ॉल्यूशन टी 2-भारित टोमोग्राम।
बिना कंट्रास्ट के T1 मोड में, VS की कल्पना नहीं की जाती है। (डी) तीर ट्यूमर के स्थान को इंगित करता है, जो दिखाई नहीं दे रहा है।
टाइप II (दूसरा) न्यूरोफाइब्रोमैटोसिस (NF2)- एक ऑटोसोमल प्रमुख वंशानुगत बीमारी जो विरासत में मिली है या अनायास होती है, जिसमें कई सौम्य ट्यूमर के गठन की विशेषता होती है, मुख्य रूप से श्वानोमास और मेनिंगियोमा, केंद्रीय तंत्रिका तंत्र में और परिधीय नसों के साथ स्थानीयकृत होते हैं। नियोप्लाज्म की सौम्य प्रकृति के बावजूद, मस्तिष्क के कार्य को बाधित करने वाले निष्क्रिय इंट्राक्रैनील ट्यूमर के गठन के कारण रोग अक्सर घातक होता है। इस बीमारी का कोई चिकित्सा उपचार नहीं है, इसके अलावा, रोगियों को ट्यूमर को हटाने के लिए कई सर्जिकल हस्तक्षेपों से गुजरना पड़ता है, जो देर-सबेर बहरापन और अंधापन की ओर ले जाता है। रोग का विकास जीन क्षति से जुड़ा हुआ है एनएफ२... इस जीन में उत्परिवर्तन पूरे शरीर में छिटपुट श्वानोमास और मेनिंगियोमा के गठन और ट्यूमर के विकास से जुड़े हैं, जो पहली नज़र में, न्यूरोफाइब्रोमैटोसिस से जुड़े नहीं हैं, उदाहरण के लिए, घातक मेसोथेलियोमा।
महामारी विज्ञान
टाइप II न्यूरोफाइब्रोमैटोसिस 50 हजार नवजात शिशुओं में से 1 में होता है।
एटियलजि
NF2 जीन क्रोमोसोम 22 (22q12) की लंबी भुजा पर स्थानीयकृत होता है और एक ट्यूमर ग्रोथ सप्रेसर - प्रोटीन मर्लिन या श्वाननोमाइन के संश्लेषण को एन्कोड करता है। मर्लिन के गुण और संरचना तीन समरूप प्रोटीनों के बहुत करीब हैं - एज़्रिन, रेडिक्सिन और मोसिन (जहाँ से इसका नाम पड़ा है) एमओज़िन इज़रीन आरएडिक्सिन ली ike प्रोटे में ) ये सभी प्रोटीन झिल्ली आयोजक के रूप में कार्य करते हैं और मुख्य रूप से कोशिका कंकाल (सूक्ष्मनलिका प्रणाली) के निर्माण और कामकाज के लिए प्रदान करते हैं। न्यूरोएक्टोडर्मल मूल के कोशिका प्रसार के नियमन में इन प्रोटीनों का सबसे बड़ा महत्व है।
मर्लिन के संश्लेषण को एन्कोडिंग करने वाले एक एनएफ 2 जीन का उत्परिवर्तन सेलुलर स्तर पर खुद को प्रकट नहीं करता है, क्योंकि एलीलिक जीन कोशिका की जरूरतों के लिए पर्याप्त प्रोटीन के संश्लेषण के लिए आरएनए उत्पन्न करता है। जब यह क्षतिग्रस्त हो जाता है (दूसरी आनुवंशिक घटना के परिणामस्वरूप), सेल में सामान्य मर्लिन का संश्लेषण बंद हो जाता है, विकास विनियमन का गतिशील संतुलन प्रसार की ओर बदल जाता है और सौम्य ट्यूमर का विकास होता है।
नैदानिक तस्वीर
टाइप II न्यूरोफाइब्रोमैटोसिस में उत्पन्न होने वाले ट्यूमर सौम्य होते हैं, लेकिन टाइप I न्यूरोफाइब्रोमैटोसिस में नियोप्लाज्म की तुलना में अधिक जैविक रूप से आक्रामक होते हैं। NF2 वाले रोगियों में संबंधित घातक ट्यूमर विकसित होने की संभावना नगण्य रूप से बढ़ जाती है।
निदान
एनएफ 2 के लिए पूर्ण नैदानिक मानदंड आठवीं तंत्रिका के द्विपक्षीय न्यूरोमा हैं। इसके अलावा, एनएफ 2 का निदान एक ऐसे रोगी में निर्धारित किया जाता है जिसका इस बीमारी से सीधा संबंध है, या तो आठवीं तंत्रिका का एकतरफा न्यूरोमा, या निम्नलिखित में से दो या अधिक संकेतों का संयोजन:
- न्यूरोफिब्रोमास
- मेनिंगिओमास (एक या अधिक)
- ग्लिओमास (एक या अधिक)
- रीढ़ की हड्डी सहित श्वानोमास (एक या अधिक)
- जुवेनाइल पोस्टीरियर सबकैप्सुलर लेंटिकुलर मोतियाबिंद या लेंस अपारदर्शिता
NF2 के लगभग 80% रोगियों में Café au lait धब्बे देखे गए हैं, लेकिन निदान नहीं हैं।
इलाज
द्विपक्षीय न्यूरोमा और संरक्षित सुनवाई के साथ, छोटे आकार के ट्यूमर के साथ इलाज शुरू करने की सिफारिश की जाती है, सुनवाई हानि के साथ - बेहतर सुनवाई कान की तरफ से। यदि ट्यूमर को पूरी तरह से हटाने के बाद भी इस तरफ की सुनवाई संतोषजनक रहती है, तो दूसरे ट्यूमर को हटा दिया जाना चाहिए। यदि सुनवाई को संरक्षित नहीं किया जा सकता है, तो शेष न्यूरोमा के लिए अपेक्षित रणनीति की सिफारिश की जाती है, और यदि लक्षण बढ़ते हैं, तो ट्यूमर को आंशिक रूप से हटा दिया जाता है (बहरेपन के उच्च जोखिम के कारण)।
यदि एनएफ 2 से जुड़े न्यूरोमा और न्यूरोफिब्रोमा केवल श्रवण तंत्रिका को विस्थापित नहीं करते हैं, तो एनएफ 2 के साथ अंगूर के गुच्छों के रूप में एक ट्यूमर अक्सर 8 वीं तंत्रिका के तंतुओं के बीच फैलता है, जिससे इन रोगियों में सुनवाई को संरक्षित करना मुश्किल हो जाता है। इसके अलावा, एनएफ 2 में, ट्यूमर को अन्य कपाल नसों से अलग करना मुश्किल है, मुख्य रूप से चेहरे से।
अन्य इंट्राकैनायल नियोप्लाज्म की उपस्थिति में, उनके सर्जिकल हटाने का संकेत दिया जाता है, यदि गठन का स्थानीयकरण और आकार इसकी अनुमति देता है, या रेडियोसर्जिकल उपचार।
85.0टाइप II (दूसरा) न्यूरोफाइब्रोमैटोसिस (NF2)- एक वंशानुगत बीमारी जो मनुष्यों में ट्यूमर के विकास की भविष्यवाणी करती है।
महामारी विज्ञान
टाइप II न्यूरोफाइब्रोमैटोसिस 50 हजार नवजात शिशुओं में से 1 में होता है।
एटियलजि
NF2 जीन क्रोमोसोम 22 (22q12) की लंबी भुजा पर स्थानीयकृत होता है और एक ट्यूमर ग्रोथ सप्रेसर - प्रोटीन मर्लिन या श्वाननोमाइन के संश्लेषण को एन्कोड करता है। मर्लिन के गुण और संरचना तीन समरूप प्रोटीनों के बहुत करीब हैं - एज़्रिन, रेडिक्सिन और मोसिन (जहाँ से इसका नाम पड़ा है) एमओज़िन इज़रीन आरएडिक्सिन ली ike प्रोटे में ) ये सभी प्रोटीन झिल्ली आयोजक के रूप में कार्य करते हैं और मुख्य रूप से कोशिका कंकाल (सूक्ष्मनलिका प्रणाली) के निर्माण और कामकाज के लिए प्रदान करते हैं। न्यूरोएक्टोडर्मल मूल के कोशिका प्रसार के नियमन में इन प्रोटीनों का सबसे बड़ा महत्व है।
मर्लिन के संश्लेषण को एन्कोडिंग करने वाले एक एनएफ 2 जीन का उत्परिवर्तन सेलुलर स्तर पर खुद को प्रकट नहीं करता है, क्योंकि एलीलिक जीन कोशिका की जरूरतों के लिए पर्याप्त प्रोटीन के संश्लेषण के लिए आरएनए उत्पन्न करता है। जब यह क्षतिग्रस्त हो जाता है (दूसरी आनुवंशिक घटना के परिणामस्वरूप), सेल में सामान्य मर्लिन का संश्लेषण बंद हो जाता है, विकास विनियमन का गतिशील संतुलन प्रसार की ओर बदल जाता है और सौम्य ट्यूमर का विकास होता है।
नैदानिक तस्वीर
टाइप II न्यूरोफाइब्रोमैटोसिस में उत्पन्न होने वाले ट्यूमर सौम्य होते हैं, लेकिन टाइप I न्यूरोफाइब्रोमैटोसिस में नियोप्लाज्म की तुलना में अधिक जैविक रूप से आक्रामक होते हैं। NF2 वाले रोगियों में संबंधित घातक ट्यूमर विकसित होने की संभावना नगण्य रूप से बढ़ जाती है।
निदान
एनएफ 2 के लिए पूर्ण नैदानिक मानदंड आठवीं तंत्रिका के द्विपक्षीय न्यूरोमा हैं। इसके अलावा, एनएफ 2 का निदान उस रोगी में निर्धारित किया जाता है जिसका इस बीमारी से सीधा संबंध है, या तो आठवीं तंत्रिका का एकतरफा न्यूरोमा, या निम्नलिखित में से दो या अधिक संकेतों का संयोजन:
- मेनिंगिओमास (एक या अधिक)
- ग्लिओमास (एक या अधिक)
- रीढ़ की हड्डी सहित श्वानोमास (एक या अधिक)
- जुवेनाइल पोस्टीरियर सबकैप्सुलर लेंटिकुलर मोतियाबिंद या लेंस अपारदर्शिता
NF2 के लगभग 80% रोगियों में कैफे-औ-लैट स्पॉट देखे गए हैं, लेकिन उनका कोई नैदानिक मूल्य नहीं है।
इलाज
द्विपक्षीय न्यूरोमा और संरक्षित सुनवाई के साथ, छोटे आकार के ट्यूमर के साथ इलाज शुरू करने की सिफारिश की जाती है, सुनवाई हानि के साथ - बेहतर सुनवाई कान की तरफ से। यदि ट्यूमर को पूरी तरह से हटाने के बाद भी इस तरफ की सुनवाई संतोषजनक रहती है, तो दूसरे ट्यूमर को हटा दिया जाना चाहिए। यदि सुनवाई को संरक्षित नहीं किया जा सकता है, तो शेष न्यूरोमा के लिए अपेक्षित रणनीति की सिफारिश की जाती है, और यदि लक्षण बढ़ते हैं, तो ट्यूमर को आंशिक रूप से हटा दिया जाता है (बहरेपन के उच्च जोखिम के कारण)।
यदि एनएफ 2 से जुड़े न्यूरोमा और न्यूरोफिब्रोमा केवल श्रवण तंत्रिका को विस्थापित नहीं करते हैं, तो एनएफ 2 के साथ अंगूर के गुच्छों के रूप में एक ट्यूमर अक्सर 8 वीं तंत्रिका के तंतुओं के बीच फैलता है, जिससे इन रोगियों में सुनवाई को संरक्षित करना मुश्किल हो जाता है। इसके अलावा, एनएफ 2 में, ट्यूमर को अन्य कपाल नसों से अलग करना मुश्किल है, मुख्य रूप से चेहरे से।
अन्य इंट्राकैनायल नियोप्लाज्म की उपस्थिति में, उनके सर्जिकल हटाने का संकेत दिया जाता है, यदि गठन का स्थानीयकरण और आकार इसकी अनुमति देता है, या रेडियोसर्जिकल उपचार।
न्यूरोफाइब्रोमैटोसिस एक अनुवांशिक विकार है जो छोटे और बड़े ट्यूमर के गठन के साथ फीडर कोशिकाओं (श्वान कोशिकाओं) की असामान्य वृद्धि की विशेषता है।
ट्यूमर सौम्य या घातक हो सकता है। न्यूरोफाइब्रोमैटोसिस एक अपेक्षाकृत दुर्लभ स्थिति है, जो जन्म लेने वाले 2,500-4,000 बच्चों में से 1 को प्रभावित करती है। यह एक ऑटोसोमल प्रमुख विरासत में मिला विकार है। रोग आमतौर पर 2 मुख्य रूपों (प्रकार 1 और 2, पुराने नाम - परिधीय और केंद्रीय) में होता है।
ज्यादातर मामलों में, जन्मजात उत्परिवर्तन रोग के विकास के कारण के रूप में एक भूमिका निभाता है, लेकिन नए उत्परिवर्तन के उद्भव के परिणामस्वरूप रोग के विकास के लिए भी संभव है। आनुवंशिक विश्लेषण का उपयोग करके निदान को सटीक रूप से निर्धारित किया जा सकता है।
समस्या की उत्पत्ति का पता लगाना
न्यूरोफाइब्रोमैटोसिस एक विरासत में मिला ऑटोसोमल प्रमुख विकार है। इसका मतलब है कि जीन के एक निश्चित संयोजन के साथ, रोग माता-पिता से विरासत में मिला है। ऑटोसोमल प्रमुख वंशानुक्रम के मामले में, दोनों लिंग समान रूप से अक्सर रोग से प्रभावित होते हैं।
रोग गैर-सेक्स गुणसूत्रों पर स्थित जीनों द्वारा फैलता है - ऑटोसोम (गुणसूत्र 17 टाइप 1 न्यूरोफाइब्रोमैटोसिस के लिए सबसे विशिष्ट है, 22 टाइप 2 के लिए)।
एक और, कम आम, विकल्प नए उत्परिवर्तन का उदय है। इसका मतलब यह है कि यह रोग सबसे पहले मनुष्यों में नए उत्परिवर्तन के गठन के साथ प्रकट होता है। उसके माता-पिता या अन्य रिश्तेदार इस बीमारी से पीड़ित नहीं होते हैं, लेकिन बाद में व्यक्ति स्वयं इस बीमारी को अपने वंशजों को देता है।
रोग की किस्में
न्यूरोफाइब्रोमैटोसिस को 2 मुख्य प्रकारों में विभाजित किया गया है:
- टाइप एनएफ1वॉन रेक्लिंगहॉसन रोग के रूप में भी जाना जाता है। पूरी बीमारी 1: 3000 लोगों के अनुपात में होती है।
- टाइप एनएफ२एक दुर्लभ घटना है, 25,000 में से 1 व्यक्ति को प्रभावित करती है।
इसके अलावा, 4 और प्रकार के रोग प्रतिष्ठित हैं, लेकिन वे अत्यंत दुर्लभ हैं और उनके उपचार की योजना दूसरे प्रकार की बीमारी के उपचार से भिन्न नहीं है।
दोनों प्रकार के अलग-अलग रोग होते हैं जिनके अलग-अलग कारण और लक्षण होते हैं।

लक्षण और अभिव्यक्तियाँ
दोनों प्रकार के रोग अलग-अलग तरीकों से प्रकट होते हैं और नैदानिक तस्वीर की प्रकृति अलग होती है।
वॉन रेक्लिंगहॉसन रोग
रेक्लिंगहॉसन न्यूरोफाइब्रोमैटोसिस बच्चों में ही प्रकट होता है और इसके निम्नलिखित लक्षण होते हैं:
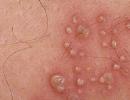
- सफेद कॉफी चरित्र त्वचा पैच... त्वचा पर हल्के भूरे रंग के धब्बे दर्द रहित होते हैं। बचपन में धब्बे 5 मिमी तक बढ़ते हैं, किशोरावस्था में - वे आकार में 15 मिमी तक बढ़ जाते हैं।
- झाईयांइस प्रकार के साथ, वे असामान्य स्थानों में होते हैं, उदाहरण के लिए, त्वचा की परतों में।
- सौम्य त्वचा ट्यूमर - neurofibromas... ये सौम्य ट्यूमर हैं जो त्वचा के नीचे बढ़ते हैं। बचपन में वे छोटे होते हैं, बढ़ती उम्र के साथ, एक नियम के रूप में, वे बड़े हो जाते हैं। न्यूरोफिब्रोमा की संख्या एक व्यक्ति से दूसरे व्यक्ति में भिन्न होती है, कुछ में, ये ट्यूमर पूरे शरीर को कवर करते हैं। उनमें से कुछ लगातार खुजली, आकार परिवर्तन या अंगों की शिथिलता का कारण बनते हैं।
- ऑप्टिक तंत्रिका ग्लियोमा... ग्लियोमा ऑप्टिक तंत्रिका का एक सौम्य ट्यूमर है जो दृश्य हानि का कारण बनता है और बच्चों में यह रंग धारणा में बदलाव का कारण बनता है।
- लिशा के पिंड... वे आंख के परितारिका पर भूरे रंग के धब्बे होते हैं।
- उच्च रक्त चाप.
- परिधीय तंत्रिका म्यान के घातक नवोप्लाज्म... प्रत्येक तंत्रिका का अपना म्यान होता है। यदि न्यूरोफिब्रोमा अचानक सूज जाता है, दर्दनाक हो जाता है, कमजोरी, मनोदशा में परिवर्तन और चरम सीमाओं में झुनझुनी दिखाई देती है, तो दुर्दमता का संदेह मौजूद होता है।

टाइप 2 न्यूरोफाइब्रोमैटोसिस
इस प्रकार के विकार की पहली अभिव्यक्ति आमतौर पर 20 वर्ष की आयु के बाद होती है, छोटे बच्चों में, रोग आमतौर पर कोई लक्षण नहीं पैदा करता है।
विशिष्ट लक्षणों में, निम्नलिखित उल्लंघन नोट किए गए हैं: 
- सुनवाई हानि, भनभनाहट और कानों में झुनझुनी;
- संतुलन बनाए रखने में समस्याएं;
- चक्कर आना और उल्टी अक्सर मौजूद होती है;
- कान के क्षेत्र में ट्यूमर की वृद्धि जो सुनवाई को नुकसान पहुंचाती है और तंत्रिकाओं का संतुलन जो मस्तिष्क को संकेत संचारित करती है।
कुछ लोगों में, यह सीधे मस्तिष्क में बढ़ता है, लेकिन हमेशा प्रकट नहीं होता है; हम सौम्य नियोप्लाज्म के बारे में बात कर रहे हैं। समस्या तब पैदा होती है जब ट्यूमर बड़े आकार में बढ़ जाता है और आसपास के मस्तिष्क के ऊतकों को दबा देता है। यह खुद को सिरदर्द, चक्कर आना, उल्टी के रूप में प्रकट कर सकता है।
वे भी विकसित हो सकते हैं, जो पैदा कर सकते हैं:
- पीठ दर्द;
- मांसपेशियों में कमजोरी;
- अंगों में झुनझुनी, सुन्नता।
NF2 में सौम्य ट्यूमर उभरी हुई त्वचा की तरह दिखते हैं जो लगभग 2 सेमी व्यास को कवर करती है।
दुर्लभ प्रकार के रोग की अभिव्यक्ति
अन्य प्रकार के न्यूरोफाइब्रोमैटोसिस के लक्षण:
- रोग 3 प्रकारकई त्वचा न्यूरोफिब्रोमा की घटना की विशेषता है, जिससे ऑप्टिक तंत्रिका ग्लियोमा, न्यूरोलेम्मा और हो सकता है;
- 4 प्रकाररोग खंडीय है, और त्वचा के केवल एक विशिष्ट क्षेत्र को प्रभावित करता है;
- न्यूरोफाइब्रोमेटोसिस 5 प्रकारन्यूरोफिब्रोमा की अनुपस्थिति की विशेषता और केवल काले धब्बे की उपस्थिति से प्रकट होता है;
- 6 प्रकाररोग की विशेषता 20 वर्ष की आयु के बाद उपस्थिति (जैसा कि टाइप 2 न्यूरोफाइब्रोमैटोसिस के मामले में) है। न्यूरोफिम दिखाई देते हैं; रोग सबसे अधिक बार अधिग्रहित किया जाता है।

नैदानिक मानदंड और आनुवंशिक विश्लेषण and
न्यूरोफाइब्रोमैटोसिस का निदान करते समय, यह जानना महत्वपूर्ण है कि हम विभिन्न अभिव्यक्तियों के साथ एक वंशानुगत बीमारी के बारे में बात कर रहे हैं। इस जानकारी के आधार पर, तथाकथित। इस बीमारी के "प्रकटीकरण" में मदद करने के उद्देश्य से नैदानिक मानदंड।
मानदंड की सूची में पहला कैफ़े-औ-लैट स्पॉट ("व्हाइट कॉफ़ी") है, जिसके लिए 5 मिलीमीटर या उससे अधिक के आकार में 6 टुकड़ों या अधिक की संख्या का संकेत दिया गया है। एक अन्य विशेषता 2 या अधिक न्यूरोफिब्रोमा की उपस्थिति का सुझाव देती है, त्वचा की परतों (बगल और कमर में), और ऑप्टिक तंत्रिका ग्लियोमा में कई झाईयां।
दो या दो से अधिक लीश स्पॉट और बोन डिसप्लेसिया की उपस्थिति भी निदान में महत्वपूर्ण भूमिका निभाती है। और, अंत में, परिवार में बीमारी की आवृत्ति कम महत्वपूर्ण नहीं है, खासकर माता-पिता, भाइयों और बहनों के संबंध में। उपरोक्त लक्षणों की घटना रोगी की उम्र के साथ बढ़ जाती है।
 ज्यादातर, 4 साल की उम्र तक, बचपन में न्यूरोफाइब्रोमैटोसिस का निदान करना संभव है। आमतौर पर निदान एक विशिष्ट नैदानिक तस्वीर पर आधारित होता है, लेकिन संदेह या अनिश्चितता के मामले में, आप आनुवंशिकी की मदद का सहारा ले सकते हैं। ऐसे में बीमारी का पता लगाने के लिए डीएनए या आरएनए विश्लेषण का इस्तेमाल किया जा सकता है।
ज्यादातर, 4 साल की उम्र तक, बचपन में न्यूरोफाइब्रोमैटोसिस का निदान करना संभव है। आमतौर पर निदान एक विशिष्ट नैदानिक तस्वीर पर आधारित होता है, लेकिन संदेह या अनिश्चितता के मामले में, आप आनुवंशिकी की मदद का सहारा ले सकते हैं। ऐसे में बीमारी का पता लगाने के लिए डीएनए या आरएनए विश्लेषण का इस्तेमाल किया जा सकता है।
इस जांच के लिए परिधीय शिरापरक रक्त का संग्रह पर्याप्त है। जब यह बीमारी होने वाले माता-पिता में से किसी एक में होती है, तो प्रसवपूर्व आनुवंशिक परीक्षण संभव है, जो अक्सर एमनियोसेंटेसिस के साथ किया जाता है। इसके अलावा, आप बच्चे के निषेचन और गर्भाधान से ठीक पहले, अंडे या शुक्राणु का पूर्व-प्रत्यारोपण कर सकते हैं।
बचपन की बीमारी
3 अलग-अलग प्रकार के न्यूरोफाइब्रोमैटोसिस हैं जो बच्चे विकसित कर सकते हैं। उनमें से प्रत्येक जीन में मौजूद आनुवंशिक दोष या गर्भाधान के तुरंत बाद उत्पन्न होने के कारण विकसित होता है।
टाइप 1 न्यूरोफाइब्रोमैटोसिस जीन क्रोमोसोम 17 पर मौजूद होता है और प्रोटीन न्यूरोफाइब्रोमिन के उत्पादन को बढ़ाता है। यह प्रोटीन तंत्रिका तंत्र में कोशिका वृद्धि को नियंत्रित करने में मदद करता है। NF1 जीन के उत्परिवर्तन के परिणामस्वरूप प्रोटीन की हानि होती है और कोशिकाएं असामान्य रूप से विकसित होती हैं।
NF2 जीन गुणसूत्र 22 पर मौजूद होता है और मर्लिन प्रोटीन के उत्पादन को प्रभावित करता है। NF2 उत्परिवर्तन से प्रोटीन की हानि होती है, जिसके परिणामस्वरूप यह तंत्रिका तंत्र में अनियंत्रित कोशिका वृद्धि की ओर जाता है।
SMARCB1 जीन गुणसूत्र 22 पर मौजूद होता है और यह schwannomatosis का कारण होता है।
बाल चिकित्सा विकारों के लिए क्लिनिक की विशेषताएं
प्रत्येक प्रकार के न्यूरोफाइब्रोमैटोसिस के अलग-अलग लक्षण और लक्षण होते हैं।
पहले प्रकार की बीमारी सबसे अधिक बार एक बच्चे में प्रकट होती है। बच्चों में टाइप 1 न्यूरोफाइब्रोमैटोसिस के दिखाई देने वाले लक्षणों में शामिल हैं:

न्यूरोफाइब्रोमैटोसिस 2 (एनएफ 2) मुख्य रूप से एक बच्चे के कानों को प्रभावित करता है:
- क्रमिक सुनवाई हानि;
- टिनिटस;
- असंतुलन।
कुछ दुर्लभ मामलों में, NF2 रीढ़ की हड्डी और परिधीय नसों को भी प्रभावित कर सकता है। इस मामले में लक्षण इस प्रकार हैं:
- तेज दर्द;
- हाथ या पैर में सुन्नता या कमजोरी।
Schwannomatosis neurofibromatosis का एक दुर्लभ रूप है जो छोटे बच्चों में शायद ही कभी होता है। रोग का यह रूप आमतौर पर अधिक उम्र में विकसित होता है और रीढ़, कपाल या परिधीय नसों पर रसौली का कारण बनता है।
रोग के इस रूप की उपस्थिति में, शरीर के किसी भी भाग में पुराना दर्द हो सकता है।
आप किसी व्यक्ति की मदद कैसे कर सकते हैं?
न्यूरोफाइब्रोमैटोसिस एक अनुवांशिक बीमारी है और दुर्भाग्य से, लाइलाज है। ट्यूमर का निर्माण डीएनए में जन्मजात परिवर्तनों के आधार पर होता है और आज इस प्रक्रिया को किसी भी तरह से प्रभावित करने का कोई तरीका नहीं है।
दवा उपचार में निम्नलिखित दवाएं लेना शामिल है:
- केटोटिफेन;
- फेनकारोल;
- कोशिका विभाजन की दर को कम करने के लिए Tigazon;
 एक ट्यूमर की स्थिति में जो रोगी को परेशान करता है (स्वस्थ ऊतक में अंतर्वर्धित होने के कारण नियोप्लाज्म के क्षेत्र में दबाव होता है, जठरांत्र संबंधी मार्ग बंद हो जाता है, या ट्यूमर किसी व्यक्ति के लिए कॉस्मेटिक रूप से अप्रिय होता है), यह हो सकता है शल्य चिकित्सा द्वारा हटा दिया गया। आमतौर पर सर्जन पूरे ट्यूमर को हटाने की कोशिश करता है। हालांकि, इस बात की कोई गारंटी नहीं है कि यह कहीं और दिखाई नहीं देगा।
एक ट्यूमर की स्थिति में जो रोगी को परेशान करता है (स्वस्थ ऊतक में अंतर्वर्धित होने के कारण नियोप्लाज्म के क्षेत्र में दबाव होता है, जठरांत्र संबंधी मार्ग बंद हो जाता है, या ट्यूमर किसी व्यक्ति के लिए कॉस्मेटिक रूप से अप्रिय होता है), यह हो सकता है शल्य चिकित्सा द्वारा हटा दिया गया। आमतौर पर सर्जन पूरे ट्यूमर को हटाने की कोशिश करता है। हालांकि, इस बात की कोई गारंटी नहीं है कि यह कहीं और दिखाई नहीं देगा।
मस्तिष्क में ट्यूमर समस्याग्रस्त हैं, जो मस्तिष्क के महत्वपूर्ण क्षेत्रों को दबा सकते हैं और दृष्टि, श्रवण, मोटर प्रणाली की विनाशकारी जटिलताओं का कारण बन सकते हैं, और पक्षाघात या सिरदर्द को ट्रिगर कर सकते हैं।
सिर के क्षेत्र में, खोपड़ी को खोलकर और ट्यूमर को हटाकर सर्जिकल हस्तक्षेप को खोलने के अलावा, आप गामा चाकू का विकल्प भी चुन सकते हैं जो विकिरण के साथ नियोप्लाज्म पर कार्य करता है। यदि सौम्य ट्यूमर घातक मेटास्टेस में विकसित होते हैं, तो कीमोथेरेपी, विकिरण चिकित्सा, और ऑन्कोलॉजी में उपयोग किए जाने वाले अन्य तरीकों की सिफारिश की जा सकती है।
माध्यमिक दुर्दमता (विकिरण के बाद एक नए ट्यूमर का निर्माण) की घटना के कारण विकिरण चिकित्सा को आमतौर पर खारिज कर दिया जाता है। उपचार का लक्ष्य रोगी की चिकित्सा जांच, नियमित जांच और, यदि आवश्यक हो, शीघ्र उपचार के साथ रोग का शीघ्र पता लगाना है।
सर्जिकल हटाने के बाद कीमोथेरेपी आमतौर पर पहली पसंद होती है। हड्डी की विकृति को सर्जिकल मजबूती या कॉस्मेटिक सुधार के साथ समायोजित किया जा सकता है।
उपरोक्त सभी उपचार केवल जीवन की गुणवत्ता में सुधार, दर्द या मानसिक पीड़ा को दूर करने का काम करते हैं, लेकिन बीमारी को पूरी तरह से ठीक नहीं करते हैं।
लोक उपचार के साथ न्यूरोफाइब्रोमैटोसिस के उपचार के लिए, चिकित्सक प्रोपोलिस टिंचर (100 ग्राम प्रोपोलिस प्रति 500 मिलीलीटर शराब) लेने की सलाह देते हैं। इसे एक सप्ताह के लिए एक अंधेरी जगह में डाला जाता है, जिसके बाद इसे फ़िल्टर किया जाना चाहिए। 30 बूँदें रोजाना 3 बार लें। टिंचर को कमरे के तापमान पर एक अंधेरी जगह में स्टोर करें।
रोग खतरनाक क्यों है?
न्यूरोफाइब्रोमैटोसिस के साथ रहना, विशेष रूप से पहले प्रकार के, बहुत तनावपूर्ण और परेशानी भरा होता है, क्योंकि यह रोग होता है  उपस्थिति पर विनाशकारी प्रभाव। रोग का नकारात्मक मनोवैज्ञानिक प्रभाव पड़ता है, भले ही यह त्वचा की उपस्थिति का केवल एक छोटा सा विरूपण हो।
उपस्थिति पर विनाशकारी प्रभाव। रोग का नकारात्मक मनोवैज्ञानिक प्रभाव पड़ता है, भले ही यह त्वचा की उपस्थिति का केवल एक छोटा सा विरूपण हो।
यह उन किशोरों के लिए विशेष रूप से सच है जो अपनी उपस्थिति के प्रति बहुत संवेदनशील हैं, रोग की अभिव्यक्तियाँ शर्म की भावना पैदा करती हैं और अवसाद और चिंता का कारण बनती हैं।
इसके अलावा, जटिलताएं अधिक गंभीर हो सकती हैं: ट्यूमर के ऊतक बहुत तेज़ी से बढ़ने लगते हैं और इसकी कोशिकाएं शरीर के अन्य भागों (मेटास्टेसिस) में फैल जाती हैं।
खतरनाक बीमारी का सामना कैसे न करें?
न्यूरोफाइब्रोमैटोसिस के लिए निवारक उपाय एक जटिल मुद्दा है जिसमें कई विकल्प शामिल हैं। जन्मजात विकार के मामले में, इसके विकास को रोकने के लिए एक सौ प्रतिशत तरीका ज्ञात नहीं है।
यदि न्यूरोफाइब्रोमैटोसिस का पारिवारिक इतिहास है, तो बच्चे की योजना बनाने वाले जोड़े के लिए आनुवंशिक विश्लेषण की संभावना है। एक परिवार का पेड़ बनाना और पहले से ही बीमार सभी लोगों को चिह्नित करना आवश्यक है।
यह जानना भी अच्छा है कि अजन्मे बच्चे की परीक्षा के प्रसवपूर्व आनुवंशिक निदान के ढांचे में हम किस प्रकार की बीमारी के बारे में बात कर रहे हैं। प्रीइम्प्लांटेशन आनुवंशिक परीक्षण गर्भाशय में आरोपण से पहले भ्रूण की जांच करने में सक्षम है।
यदि हम जीवन भर के दौरान प्राप्त की गई बीमारी के बारे में बात कर रहे हैं, तो सैद्धांतिक रूप से उन सभी चीजों से बचना संभव है जो मानव आनुवंशिकी (विकिरण, रासायनिक और विषाक्त पदार्थ, आदि) को प्रभावित कर सकती हैं, लेकिन दुर्भाग्य से, सफलता की गारंटी के बिना।
रोग को रोकने की उपरोक्त संभावनाएं कुछ अलौकिक लग सकती हैं, लेकिन, इसके बावजूद, वे कुछ हद तक सीमित हैं, और हमेशा रोग के विकास को 100% तक नहीं रोक सकते हैं।
(एनएफ) एक वंशानुगत बीमारी है जो मनुष्यों में ट्यूमर के विकास की भविष्यवाणी करती है।
साहित्य में, न्यूरोफाइब्रोमैटोसिस का वर्णन पहली बार 1822 में स्कॉटिश सर्जन विशार्ट द्वारा किया गया था, जिन्होंने टाइप 2 एनएफ वाले रोगी का वर्णन किया था। टाइप 1 न्यूरोफाइब्रोमैटोसिस का अध्ययन और वर्णन 1882 में विरचो के छात्र वॉन रेकलिंगहौसेन द्वारा किया गया था। हालांकि, 1916 में, कुशिंग ने अपने वैज्ञानिक कार्यों में इन बीमारियों को सामान्य नाम "रेक्लिंगहॉसन रोग" के तहत संयोजित किया, और आणविक आनुवंशिक अध्ययन के बाद ही, जिसके परिणाम 1985 और 1987 में प्रकाशित हुए, NF1 और NF2 के रोगजनन में मूलभूत अंतर थे। प्रकट किया। यह साबित हो गया है कि ये पूरी तरह से अलग बीमारियां हैं जिनके लिए एक विभेदित नैदानिक दृष्टिकोण की आवश्यकता होती है।
साहित्य न्यूरोफाइब्रोमैटोसिस के केवल आठ "प्रकारों" का वर्णन करता है, लेकिन हाल ही में उनमें से अधिकांश (एनएफ 2 को छोड़कर) को एनएफ 1 के गर्भपात रूप माना जाता है और स्वतंत्र नोसोलॉजिकल रूपों के रूप में प्रतिष्ठित नहीं हैं। अपवाद खंडीय neurofibromatosis (NF5) हो सकते हैं, जब NF1 की विशिष्ट अभिव्यक्तियाँ एक या अधिक आसन्न त्वचीय (अत्यंत दुर्लभ, आमतौर पर विरासत में नहीं) में स्थानीयकृत होती हैं, और, आठ की संख्या में शामिल नहीं, स्पाइनल न्यूरोफाइब्रोमैटोसिस, जिसमें सभी रीढ़ की हड्डी की जड़ें होती हैं सममित रूप से प्रभावित (केवल कुछ टिप्पणियों का वर्णन किया गया है)।
टाइप 1 न्यूरोफाइब्रोमैटोसिस (NF1) एक ऑटोसोमल प्रमुख विकार है (जनसंख्या में घटना 3500 नवजात शिशुओं में 1 है)। NF1 के सभी मामलों में, आनुवंशिक दोष गुणसूत्र 17 (17q11.2) के क्षेत्र 11.2 में स्थानीयकृत है। यहां स्थित NF1 जीन एक बड़े प्रोटीन - न्यूरोफाइब्रोमिन के संश्लेषण को एन्कोड करता है, जो प्रमोटर प्रोटीन (रास-प्रोटीन और इसके एनालॉग्स) को निष्क्रिय करने में शामिल होता है, जो कोशिका वृद्धि का गतिशील नियंत्रण प्रदान करता है। एनएफ1 जीन मुख्य रूप से न्यूरोएक्टोडर्मल मूल के लगभग 30% शरीर के ऊतकों के लिए मुख्य ट्यूमर शमन जीन में से एक है। जब एनएफ 1 जीन जोड़ी 17 के गुणसूत्रों में से एक में क्षतिग्रस्त हो जाता है, तो संश्लेषित न्यूरोफिब्रोमिन का 50% दोषपूर्ण हो जाता है, और प्रसार की ओर कोशिका वृद्धि के संतुलन में बदलाव देखा जाता है।
हम टाइप 2 न्यूरोफाइब्रोमैटोसिस पर ध्यान केंद्रित करना चाहते हैं, जिसे पहले "सेंट्रल न्यूरोफाइब्रोमैटोसिस" कहा जाता था और जो केंद्रीय तंत्रिका तंत्र में सौम्य नियोप्लाज्म की उपस्थिति का अनुमान लगाता है।
न्यूरोफाइब्रोमैटोसिस टाइप 2 (एनएफ 2), एनएफ 1 की तरह, एक ऑटोसोमल प्रमुख बीमारी है, लेकिन यह आबादी में बहुत कम होती है (प्रति 40,000 नवजात शिशुओं में 1 मामला)। इस रोग में आनुवंशिक दोष मूल रूप से एक अलग गुणसूत्र में होता है और इसलिए इस रोग का रोगजनन अलग होता है।
HF2 जीन क्रोमोसोम 22 (22q12) पर स्थानीयकृत है और एक अन्य ट्यूमर ग्रोथ सप्रेसर, प्रोटीन मर्लिन के संश्लेषण को एन्कोड करता है, जो एक झिल्ली आयोजक के रूप में कार्य करता है और मुख्य रूप से सेल कंकाल के निर्माण और कामकाज को सुनिश्चित करता है। न्यूरोएक्टोडर्मल मूल के कोशिका प्रसार के नियमन में इस प्रोटीन का सबसे बड़ा महत्व है।
एक गुणसूत्र में NF2 जीन एन्कोडिंग मर्लिन संश्लेषण का उत्परिवर्तन सेलुलर स्तर पर खुद को प्रकट नहीं करता है, क्योंकि मर्लिन संश्लेषण में 50% की कमी ईआरएम प्रोटीन द्वारा समतल की जाती है, जो सेल प्रसार के नियमन में भी शामिल हैं। हालांकि, जब HF2 एलील जीन क्षतिग्रस्त हो जाता है ("दूसरी आनुवंशिक घटना" के परिणामस्वरूप - गुणसूत्र 22 पर सममित उत्परिवर्तन या हेटेरोज़ायोसिटी की हानि), सेल में सामान्य मर्लिन का संश्लेषण बंद हो जाता है, विकास विनियमन का गतिशील संतुलन बदल जाता है प्रसार और सौम्य ट्यूमर वृद्धि होती है।
रोगियों में कई गैर-विशिष्ट लक्षणों की उपस्थिति को देखते हुए, 1987 में "NF2" के निदान के लिए, यूएस नेशनल इंस्टीट्यूट ऑफ हेल्थ ने पूर्ण नैदानिक मानदंड (NIH मानदंड) विकसित किया, और बाद में उनके लिए संभावित मानदंड जोड़े (तालिका 1)।
तालिका 1. neurofibromatosis टाइप 2 के लिए नैदानिक मानदंड (एनआईएच मानदंड और संभावित मानदंड शामिल हैं)।
निरपेक्ष संकेत | संभावित संकेत |
||
द्विपक्षीय वेस्टिबुलर श्वानोमास (आठवीं कपाल तंत्रिका का न्यूरिनोमा) | परिवार के इतिहास | एकतरफा वेस्टिबुलर श्वानोमा आयु 30 वर्ष से कम इनमें से कोई भी दो (मेनिन्जियोमा, ग्लियोमा, न्यूरोफिब्रोमा, श्वानोमा, पोस्टीरियर सबकैप्सुलर लेंटिकुलर मोतियाबिंद) | एकाधिक मेनिंगियोमा (दो या अधिक) एकतरफा वेस्टिबुलर श्वानोमा इनमें से दो या अधिक ट्यूमर (ग्लियोमा, न्यूरोफिब्रोमा, श्वानोमा) या मोतियाबिंद |
एंटिनहाइमो एट अल के अनुसार, श्वानोमास वाले 3% रोगियों और मेनिंगियोमा के 1% रोगियों में न्यूरोफाइब्रोमैटोसिस होता है। कई मेनिंगियोमा वाले 20% रोगियों में NF2 [2] होता है।
रोग की नैदानिक अभिव्यक्ति।
टाइप 2 न्यूरोफाइब्रोमैटोसिस की सबसे आम अभिव्यक्ति द्विपक्षीय वेस्टिबुलर श्वानोमास की उपस्थिति है। दूसरे सबसे आम ट्यूमर अन्य कपाल, रीढ़ की हड्डी और परिधीय नसों के श्वानोमा हैं। बहुत कम बार (10% से कम) मेनिंगिओमास (इंट्राक्रानियल, ऑप्टिक नसों और रीढ़ की हड्डी के मेनिंगियोमास सहित), एपिंडिमोमा और ग्लियोमा हैं।
सिद्धांत रूप में, श्वानोमा शरीर में कहीं भी बन सकता है जहां श्वान कोशिकाओं के साथ तंत्रिकाएं होती हैं। NF2 में आठवीं तंत्रिका पर ट्यूमर का पसंदीदा स्थानीयकरण आज भी अस्पष्टीकृत है।
ज्यादातर, रोगी सुनवाई हानि या टिनिटस की उपस्थिति के संबंध में डॉक्टर के पास जाते हैं, जो रोग की शुरुआत में एकतरफा होते हैं। ये शिकायतें चक्कर आना और गतिभंग के साथ हो सकती हैं। इन रोगियों में 20-30% मामलों में, वेस्टिबुलर श्वानोमास के अलावा, मेनिंगियोमा, रीढ़ की हड्डी या परिधीय ट्यूमर का पता लगाया जाता है।
अक्सर, रोग बेल के पक्षाघात (3-5%) के साथ प्रकट होता है, जो उपचार का जवाब नहीं देता है और इसके प्रकट होने के कारण की पहचान से पहले कई साल बीत जाते हैं। कुछ रोगियों में पोलियोमाइलाइटिस जैसा सिंड्रोम (लगभग 3%) विकसित हो जाता है।
टाइप 2 न्यूरोफाइब्रोमैटोसिस वाले 60-80% रोगियों में दृश्य हानि होती है - मोतियाबिंद, रेटिनोब्लास्टोमा, हेमार्थ्रोमा, ऑप्टिक नसों के मेनिंगियोमा आदि।
लगभग 70% रोगियों में परिधीय नसों (कॉफी और दूध के धब्बे, श्वानोमास, न्यूरोफिब्रोमास) की त्वचा और बाहर की शाखाओं में परिवर्तन होते हैं।
न्यूरोफाइब्रोमैटोसिस टाइप 2 के साथ मेनिंगियोमा अधिक बार स्थानीयकृत होते हैं और मुख्य रूप से ललाट और पार्श्विका क्षेत्रों में सिकल प्रक्रिया पर स्थित होते हैं। एक विशेष प्रकार के मेनिन्जियोमा की घटना में कोई नियमितता की पहचान नहीं की गई है। स्पाइनल मेनिंगियोमा की उपस्थिति भी विशेषता है। मेनिन्जियोमा के हिस्टोलॉजिकल प्रकार और NF2 की उपस्थिति के बीच कोई संबंध नहीं पाया गया।
NF2 और मेनिंगियोमा के बारंबार संयोजन को एक गुणसूत्र पर आनुवंशिक दोष की उपस्थिति से समझाया गया है। छिटपुट मेनिंगियोमा में, गुणसूत्र 22 में NF2 जीन में उत्परिवर्तन 30-60% में होता है।
मेनिंगियोमा और श्वानोमा कोशिकाओं से युक्त मिश्रित ट्यूमर के मामलों का वर्णन किया गया है। एक नियम के रूप में, ये ट्यूमर अनुमस्तिष्क कोण के क्षेत्र में स्थानीयकृत होते हैं। इसके अलावा, एनएफ 2 के साथ, मेनिंगोएंजियोमैटोसिस का अक्सर पता लगाया जाता है।
8% मामलों में, आठवीं कपाल तंत्रिका के न्यूरोमा की उपस्थिति से पहले मेनिंगियोमा पहले नियोप्लाज्म होते हैं। मेनिंगिओमास वाले रोगियों की आनुवंशिक जांच अक्सर (90% मामलों में) गुणसूत्र 22 में एक उत्परिवर्तन का खुलासा करती है।
NF2 में निम्न-श्रेणी के एपिन्डिमोमा और ग्लियोमा बहुत कम आम हैं, और ट्यूमर मुख्य रूप से ब्रेनस्टेम और रीढ़ की हड्डी के ऊपरी ग्रीवा क्षेत्रों में स्थानीयकृत होते हैं। इन ट्यूमर की दुर्दमता दुर्लभ है और ज्यादातर मामलों में, विकिरण चिकित्सा से जुड़ी होती है।
सर्जिकल रणनीति।
द्विपक्षीय न्यूरोमा और संरक्षित सुनवाई के साथ, छोटे आकार के ट्यूमर के साथ इलाज शुरू करने की सिफारिश की जाती है, सुनवाई हानि के मामले में - बेहतर सुनवाई कान की तरफ से। यदि ट्यूमर को पूरी तरह से हटाने के बाद भी इस तरफ की सुनवाई संतोषजनक रहती है, तो दूसरे ट्यूमर को हटा दिया जाना चाहिए। यदि सुनवाई को संरक्षित नहीं किया जा सकता है, तो शेष न्यूरोमा के लिए अपेक्षित रणनीति की सिफारिश की जाती है, और यदि लक्षण बढ़ते हैं, तो ट्यूमर को आंशिक रूप से हटा दिया जाता है (बहरेपन के उच्च जोखिम के कारण)।
यदि एनएफ 2 से जुड़े न्यूरोमा और न्यूरोफिब्रोमा केवल श्रवण तंत्रिका को विस्थापित नहीं करते हैं, तो एनएफ 2 के साथ अंगूर के गुच्छों के रूप में एक ट्यूमर अक्सर 8 वीं तंत्रिका के तंतुओं के बीच फैलता है, जिससे इन रोगियों में सुनवाई को संरक्षित करना मुश्किल हो जाता है। इसके अलावा, एनएफ 2 में, ट्यूमर को अन्य कपाल नसों से अलग करना मुश्किल है, मुख्य रूप से चेहरे से।
अन्य इंट्राकैनायल नियोप्लाज्म की उपस्थिति में, उनके सर्जिकल हटाने का संकेत दिया जाता है, यदि गठन का स्थानीयकरण और आकार इसकी अनुमति देता है, या रेडियोसर्जिकल उपचार।
अभ्यास से मामला
यहां एनएफ 2 और कई इंट्राक्रैनील और एक्स्ट्राक्रानियल द्रव्यमान वाले रोगी के सफल उपचार का विवरण दिया गया है।
रोगी एल।, 27 वर्ष, रूसी चिकित्सा विज्ञान अकादमी के रसायन विज्ञान के रिपब्लिकन वैज्ञानिक केंद्र के राज्य संस्थान के न्यूरोसर्जिकल विभाग में अस्पताल में भर्ती। बी.वी. पेत्रोव्स्की 03/29/2006 सिरदर्द की शिकायत जो सुबह बढ़ जाती है और जब आगे झुकते हैं, तो दाहिनी ओर एक्सोफथाल्मोस, दाहिनी आंख में दर्द, दृष्टि में कमी, दोहरी दृष्टि, नाक के दाहिने आधे हिस्से की आवर्तक "भीड़"।
इतिहास से ज्ञात होता है कि लगभग ६ माह पूर्व रोगी को दायीं ओर एक छोटा एक्सोफ्थाल्मोस मिला, जिसके लिए निवास स्थान पर नेत्र रोग विशेषज्ञों द्वारा उसकी जांच की गई और उसका उपचार किया गया, लेकिन एक्सोफथाल्मोस बढ़ गया। 2-3 महीनों के बाद, सिरदर्द दिखाई दिया, ललाट क्षेत्र और आंख के सॉकेट के क्षेत्र में स्थानीयकृत, जो एनएसएआईडी के सेवन से राहत नहीं मिली थी। धीरे-धीरे सिरदर्द बढ़ता गया, समय-समय पर, बिना किसी कारण के, नाक से सांस लेने में कठिनाई दाईं ओर दिखाई देने लगी। एक आउट पेशेंट के आधार पर, मस्तिष्क की सीटी का प्रदर्शन किया गया, जिसमें ललाट क्षेत्र के बेसल भागों में एक द्रव्यमान का पता चला, जो एथमॉइड भूलभुलैया के माध्यम से नाक गुहा में फैल गया, और औसत दर्जे की दीवार के माध्यम से दाहिनी कक्षा की गुहा में बढ़ रहा था। पारिवारिक इतिहास बोझ नहीं है, रोगी के रिश्तेदारों के बीच अब तक किसी भी ऑन्कोलॉजिकल रोगों की पहचान नहीं की गई है।
प्रवेश पर रोगी की सामान्य स्थिति संतोषजनक है। रोगी की दैहिक स्थिति में कोई विकृति प्रकट नहीं हुई थी।
न्यूरोलॉजिकल स्थिति:चेतना स्पष्ट, उन्मुख, पर्याप्त है। जीसीएस - 15 अंक। मेनिन्जियल लक्षण नहीं होते हैं। दाएं तरफा एक्सोफ्थाल्मोस, विद्यार्थियों ओएस = ओडी, फोटोरिएक्शन और कॉर्नियल रिफ्लेक्सिस ज्वलंत हैं। दाहिने नेत्रगोलक के ऊपर और औसत दर्जे की गति का प्रतिबंध, दाईं ओर बिगड़ा हुआ अभिसरण, डिप्लोपिया। विसस ओडी = 0.7, ओएस = 1. चेहरा सममित है, जीभ मध्य रेखा में है। छोरों से टेंडन रिफ्लेक्सिस कुछ हद तक बाईं ओर पुनर्जीवित होते हैं, मांसपेशियों की टोन पक्षों में अंतर के बिना। कोई पैरेसिस या संवेदी गड़बड़ी नहीं है। इरादे से समन्वय परीक्षण करता है।
रोगी की जांच करते समय, दाएं तरफा एक्सोफथाल्मोस पर ध्यान आकर्षित किया जाता है, बाईं नेत्रगोलक की गति दर्दनाक होती है, दाईं ओर वे कुछ हद तक ऊपर और मध्य में सीमित होती हैं। नाक की पार्श्व दीवार पर, शीर्ष पर, दाहिनी आंख के सॉकेट के पास, त्वचा के नीचे, चिकनी किनारों के साथ एक घनी स्थिरता का गठन स्पष्ट है। दाहिने हाथ की हथेली की सतह पर एक गोल आकार का एक चमड़े के नीचे का गठन होता है, जिसकी माप 0.7 x 0.5 x 0.5 सेमी होती है, जो त्वचा से विस्थापित नहीं होती है और पैल्पेशन पर मध्यम रूप से दर्दनाक होती है। बाएं हाथ की दूसरी उंगली के मध्य भाग पर और पश्चकपाल क्षेत्र में समान चमड़े के नीचे की संरचनाएं पाई गईं।
फंडस पर कोई पैथोलॉजी नहीं पाई गई।
एक ओटोलरींगोलॉजिस्ट द्वारा रोगी की जांच की गई - दाहिने नाक के मार्ग की पार्श्व दीवार पर, पीछे के ऊपरी हिस्सों में, नाक के मार्ग की गुहा में 4-5 मिमी के घने सबम्यूकोसल गठन का पता चला था।
रोगी ने इसके विपरीत मस्तिष्क का एमआरआई कराया, जिससे पता चला:
एथमॉइड हड्डी के प्रक्षेपण में, परिवर्तित एमआर सिग्नल का एक अमानवीय क्षेत्र प्रकट होता है (टी 1-भारित छवियों पर हाइपोटेंस और टी 2-भारित छवियों पर हाइपरिंटेंस) 77 x 35 x 39 मिमी के कुल आकार के साथ, अनियमित आकार में फैल के साथ दाहिनी कक्षा (आंतरिक और ऊपरी तिरछी आंख की मांसपेशियों के संपीड़न और विस्थापन के साथ नेत्रगोलक के बाहरी और बाहरी विस्थापन के साथ) और दाईं ओर ऊपरी नासिका मार्ग (हड्डी संरचनाओं के विनाश के साथ), ललाट साइनस और दाएं के कोमल ऊतकों में नाक का आधा भाग। कपाल गुहा में अतिरिक्त रूप से विस्तार करते हुए, गठन ललाट लोब को पीछे और बाद में संकुचित और विस्थापित करता है। घाव के इंट्राक्रैनील भाग से एमआर संकेत टी1 और टी2-भारित छवियों में तेजी से बढ़ा है।
इंटरहेमिस्फेरिक सल्कस के ललाट भागों में, स्पष्ट सम आकृति के साथ एक गोल संरचना निर्धारित की जाती है, जो मस्तिष्क के अर्धचंद्र से निकलती है, T1 और T2 छवियों पर आइसोइंटेंस है। गठन का आकार लगभग 8 मिमी है।
क्रैनियोवर्टेब्रल जंक्शन के स्तर पर, रीढ़ की हड्डी की नहर के अंदर बाईं ओर और मज्जा ऑबोंगटा के पीछे, इसके निकट, एक गोल आकार का वॉल्यूमेट्रिक द्रव्यमान जिसमें स्पष्ट समरूपता भी निर्धारित की जाती है, आयामों के साथ T1 और T2-भारित छवियों पर आइसोइंटेंसिव 6 x 10 मिमी।
एक विपरीत एजेंट की शुरूआत के बाद, नाक और परानासल साइनस के क्षेत्र में शिक्षा का तीव्र विषम संचय नोट किया जाता है। अन्य संरचनाएं समान रूप से विपरीत जमा करती हैं। एमआरआई डेटा को विशेषज्ञों द्वारा पॉलीपोसिस (?) के रूप में माना जाता है जो माध्यमिक माइकोटिक संक्रमण और रक्तस्राव से जटिल होता है।
एक अतिरिक्त परीक्षा के बाद, 6 अप्रैल, 2006 को, रोगी की सर्जरी हुई - ललाट क्षेत्र में ऑस्टियोप्लास्टिक ट्रेपनेशन, दाहिने ललाट क्षेत्र में एक छोटे उत्तल मेनिंगियोमा को हटाना (ऑपरेशन के दौरान पहचाना गया), पूर्वकाल तीसरे के मेनिंगियोमा को हटाना फाल्कस, क्रानियोफेशियल मास फॉर्मेशन को हटाना।
सामान्य संज्ञाहरण के तहत, एल 3-एल 4 अंतराल में एक काठ का नाली स्थापित किया जाता है, और एक पारदर्शी, रंगहीन मस्तिष्कमेरु द्रव नाली के माध्यम से बहता है। ललाट क्षेत्र में कोमल ऊतकों में एक धनुषाकार चीरा बनाया गया था। ऑस्टियोप्लास्टिक ट्रेपनेशन ललाट क्षेत्र में ललाट की हड्डी के अतिरिक्त उच्छेदन और ललाट साइनस की दीवारों से पूर्वकाल कपाल फोसा के नीचे तक किया गया था। ड्यूरा मेटर तनावपूर्ण है, पूर्वकाल कपाल फोसा के तल पर, एक बड़ा घाव अतिरिक्त रूप से पड़ा हुआ पाया गया था। ड्यूरा मेटर के शीर्ष पर दाहिने ललाट क्षेत्र में, एक चाप खोला गया था और एक छोटा उत्तल मेनिंगियोमा पाया गया था, जिसे इसके प्रारंभिक विकास के स्थान पर ड्यूरा मेटर की लकीर के साथ हटा दिया गया था। एक इंटरहेमिस्फेरिक दृष्टिकोण का उपयोग फाल्क्स के पूर्वकाल तीसरे के मेनिंगियोमा से संपर्क करने के लिए किया गया था, जो 1.5 सेमी की गहराई पर स्थित था। मेनिंगियोमा को इसके विकास के स्थान पर फाल्क्स के उच्छेदन के साथ हटा दिया गया था। ड्यूरा मेटर दोष को एपोन्यूरोसिस के साथ प्लास्टिसाइज़ किया गया था।
पूर्वकाल कपाल फोसा के तल पर ट्यूमर परिधि के साथ अलग किया गया था प्रारंभिक ट्यूमर वृद्धि का स्थान घ्राण फोसा तल का ड्यूरा मेटर था। इस जगह पर, ड्यूरा मेटर को एक्साइज किया गया था, जिसके बाद ट्यूमर के इंट्राक्रैनील भाग को हटा दिया गया था, जो एक ठोस घटक और घनी दीवारों वाला एक पुटी था। ललाट साइनस की गुहा ट्यूमर के एक ठोस घटक से भर गई थी, जिसे हटा दिया गया था, ललाट साइनस से श्लेष्म झिल्ली को भी हटा दिया गया था। इसके अलावा, एथमॉइड हड्डी की क्षैतिज प्लेट का उच्छेदन किया गया था, ट्यूमर द्वारा अंकुरित एथमॉइड भूलभुलैया का उच्छेदन। कपाल गुहा से गांठ लगाकर ट्यूमर के इंट्रानैसल भाग को हटा दिया गया था, और ट्यूमर को हटाने के बाद, बेहतर शंख के स्तर पर कपाल गुहा से नाक गुहा तक एक सीधा मार्ग बनाया गया था। इस दृष्टिकोण से ट्यूमर के अंतर्गर्भाशयी भाग को भी हटा दिया गया था। रक्तचाप पर हेमोस्टेसिस 150/90 मिमी एचजी
ड्यूरा मेटर के दोष को फाइब्रिन गोंद टिसुकोल - किट के साथ फ्लैप की परिधि के साथ ग्लूइंग के साथ एपोन्यूरोसिस की दो परतों के साथ प्लास्टिसाइज़ किया गया था। ऑपरेशन के अंत तक, मस्तिष्क डूब जाता है, अच्छी तरह से स्पंदित होता है। गठित गुहा की दीवारों को हेमोस्टैटिक धुंध "सर्जसेल" के साथ रेखांकित किया गया है। हड्डी के फ्लैप को टाइटेनियम प्लेटों के साथ तय किया गया था, खोपड़ी की हड्डी के दोष की प्राथमिक प्लास्टिक सर्जरी टाइटेनियम इम्प्लांट के साथ की गई थी। परत-दर-परत घाव बंद होना। आयोडीन, शराब, ए.सी. पट्टी। नाक के पूर्वकाल टैम्पोनैड का प्रदर्शन किया गया था।
हटाए गए नियोप्लाज्म की हिस्टोलॉजिकल जांच से मेनिंगोथेलियोमैटस मेनिंगियोमा की कोशिकाओं का पता चला।
पश्चात की अवधि में, रोगी को संवहनी, जीवाणुरोधी और विरोधी भड़काऊ दवाओं सहित विभाग में रूढ़िवादी चिकित्सा से गुजरना पड़ा। 12 दिनों तक मरीज का काठ का नाला था, जिसे बाद में हटा दिया गया। पोस्टऑपरेटिव घाव मुख्य रूप से ठीक हो गया। नाक से मस्तिष्कमेरु द्रव का रिसाव नहीं होता है, चेहरे पर कोई कॉस्मेटिक दोष नहीं होता है।
०५/०२/२००६ को, रोगी को शल्य चिकित्सा उपचार के दूसरे चरण से गुजरना पड़ा - ओसीसीपिटल हड्डी के तराजू का उच्छेदन, एटलस के पीछे के आधे-आर्क का उच्छेदन, क्रानियोवर्टेब्रल स्थानीयकरण के एक बड़े गठन को हटाने, खोपड़ी दोष का प्राथमिक प्लास्टर टाइटेनियम प्रत्यारोपण के साथ। दाहिने हाथ की ताड़ की सतह और पश्चकपाल क्षेत्र के कोमल ऊतकों पर श्वानोमा को हटाना।
सामान्य संज्ञाहरण के तहत, बाईं ओर के दृष्टिकोण के साथ ग्रीवा-पश्चकपाल क्षेत्र में नरम ऊतकों का एक रैखिक चीरा बनाया गया था। पश्चकपाल हड्डी के तराजू, एटलस के आर्च, स्पिनस प्रक्रिया और दूसरे ग्रीवा कशेरुका के आर्च को कंकालित किया गया था। पश्चकपाल हड्डी के तराजू (बाईं ओर अधिक) और एटलस के पीछे के आधे-आर्क को बचाया गया था। सेरेब्रल डक्ट को रैखिक रूप से खोला गया था, बड़े ओसीसीपिटल सिस्टर्न को खोला गया था, मस्तिष्कमेरु द्रव को छोड़ा गया था, जिसके बाद मस्तिष्क को जोड़ा गया था। बाईं ओर धड़ के दुम भाग के स्तर पर और रीढ़ की हड्डी के ऊपरी खंडों में ड्यूरा मेटर खोलने के बाद, ग्रे रंग का एक गोल आकार का बड़ा द्रव्यमान, घनी स्थिरता, आसन्न मस्तिष्क से अच्छी तरह से सीमांकित, निचोड़ना और विस्थापित करना वह ढूंढ लिए गए। ब्रेन स्टेम से निकलने वाली छोटी धमनियां ट्यूमर के औसत दर्जे के हिस्सों से कसकर जुड़ी होती हैं। माइक्रोस्कोप के तहत, धमनियों को आंशिक रूप से जमा हुआ ट्यूमर से स्पष्ट रूप से अलग किया जाता है। ट्यूमर गौण तंत्रिका की दो तंत्रिका जड़ों से विकसित हुआ। तंत्रिका जड़ों को जमाया जाता है और ट्यूमर से काट दिया जाता है, जिसके बाद ट्यूमर को हटा दिया जाता है। हटाए गए ट्यूमर का आकार 2 x 1 x 1 सेमी है। बीपी 110/70 मिमी एचजी पर हेमोस्टेसिस। ड्यूरा मेटर को बाधित टांके के साथ कसकर सिल दिया गया था। परत-दर-परत घाव बंद होना।
ऊतकीय निष्कर्ष श्वानोमा है।
परिधीय द्रव्यमान को हटाने, जो कि श्वानोमास भी निकला, का भी प्रदर्शन किया गया।
16 मई, 2006 को, रोगी को न्यूरोलॉजिकल घाटे के बिना और कॉस्मेटिक दोषों के बिना निवास स्थान पर विशेषज्ञों की देखरेख में संतोषजनक स्थिति में छुट्टी दे दी गई थी।
रोगी की जांच के आधार पर, एमआरआई डेटा, हिस्टोलॉजिकल परीक्षा डेटा, न्यूरोफिब्रोमैटोसिस 2 के पूर्ण और संभावित संकेतों को ध्यान में रखते हुए, एक आनुवंशिकीविद् के साथ, रोगी को टाइप 2 न्यूरोफिब्रोमैटोसिस, क्रानियोफेशियल मेनिंगियोमा के साथ इट्राक्रानियल रूप से फैलाया गया था - ललाट में क्षेत्र, अतिरिक्त रूप से - दाहिनी कक्षा की गुहा और नाक गुहा में ... बाज के पूर्वकाल तीसरे का मेनिंगियोमा। दाएं पार्श्विका क्षेत्र में उत्तल मेनिन्जियोमा। लेफ्ट एक्सेसरी (XI) तंत्रिका का श्वानोमा। परिधीय नसों की बाहर की शाखाओं के श्वानोमास (3)। पश्चकपाल क्षेत्र के कोमल ऊतकों का श्वानोमा।
मस्तिष्क के नियंत्रण एमआरआई 6 महीने बाद कपाल गुहा में कोई द्रव्यमान नहीं दिखा। सर्वाइकल स्पाइन के एमआरआई में कोई विकृति नहीं पाई गई।
ग्रंथ सूची।
- कोनोवलोव ए.एन., कोज़लोव ए.वी. वंशानुगत रोग खोपड़ी के आधार के ट्यूमर के विकास में योगदान करते हैं। "खोपड़ी के आधार के ट्यूमर की सर्जरी" पुस्तक में, पीपी। 169-170।
- एंटिनहाइमो जे, हापासालो एच, हल्टिया एम, टाटागिबा एम, थॉमस एस, ब्रैंडिस ए, सैनियो एम, कारपेन ओ, सामी एम, जैस्केलैनन जे। न्यूरोफिब्रोमैटोसिस 2-जुड़े और छिटपुट मेनिंगियोमा में प्रसार क्षमता और ऊतकीय विशेषताएं। जे न्यूरोसर्ज 1997; 87: 610-614।
- एंटिनहाइमो जे, सांकिला आर, कारपेन ओ, पुक्कला ई, सैनियो एम, जास्केलैनन जे। छिटपुट और एनएफ2-संबंधित मेनिंगिओमास और श्वानोमास का जनसंख्या आधारित विश्लेषण। जे न्यूरोल 2000; 54: 71-76।
- बेसर एम, माउटनर वीएफ, ठक्कर एसडी, क्लुवे एल। न्यूरोफाइब्रोमैटोसिस का प्राकृतिक इतिहास 2. एम जे हम जेनेट 1998; 63 (सप्ल 4): ए 63।
- बेसर एमई, इवांस डीजीआर, जैकलर आरके, सुजान्स्की ई, रूबेनस्टीन ए। घातक परिधीय तंत्रिका म्यान ट्यूमर, रेडियोथेरेपी, और न्यूरोफाइब्रोमैटोसिस 2. बीआर जे कैंसर 2000; 82: 998।
- बेसर एमई, फ्रीडमैन जेएम, इवांस डीजीआर। न्यूरोफाइब्रोमैटोसिस में उत्तरजीविता के भविष्यवक्ता 2. एम जे हम जेनेट 1999; 65 (सप्ल 4): ए 61।
- बेसर एमई, मौटनर वीएफ, रैग एनके, नेचिपोरुक ए, रिकार्डी वीएम, क्लेन जे, सैन्ज जे, पुलस्ट एसएम। लिंक्ड जेनेटिक मार्करों, न्यूरोइमेजिंग और ओकुलर परीक्षाओं का उपयोग करके न्यूरोफाइब्रोमैटोसिस 2 का पूर्व-लक्षण निदान। न्यूरोलॉजी 1996; 47: 1269-1277।
- काला पीएम। मेनिंगियोमास। न्यूरोसर्जरी। 1993 अप्रैल; 32 (4): 643-57।
- चक्रवर्ती ए, फ्रैंक्स एजे। Meningioangiomatosis: एक केस रिपोर्ट और साहित्य की समीक्षा। ब्र जे न्यूरोसर्ज। 1999 अप्रैल; 13 (2): 167-73।
- क्लॉस ईबी, बॉन्डी एमएल, शिल्डक्राट जेएम, वीमेल्स जेएल, रेंसच एम, ब्लैक पीएम। इंट्राक्रैनील मेनिंगियोमा की महामारी विज्ञान। न्यूरोसर्जरी। २००५ दिसंबर, ५७ (६): १०८८-९५
- क्रो एफडब्ल्यू, शूल डब्ल्यूजे, नील जेवी। मल्टीपल न्यूरोफाइब्रोमैटोसिस का क्लिनिकल पैथोलॉजिकल एंड जेनेटिक स्टडी। स्प्रिंगफील्ड, इलिनोइस: चार्ल्स सी थॉमस, 1956।
- एलिजाबेथ जे, मेनन जी, नायर एस, राधाकृष्णन वीवी। न्यूरोफाइब्रोमैटोसिस -2 वाले रोगी में श्वानोमा और मेनिंगियोमा का मिश्रित ट्यूमर: एक केस रिपोर्ट। न्यूरोल इंडिया २००१; ४९: ३९८-४००
- एलजामेल एमएस, फॉय पीएम। एकाधिक मेनिंगियोमा और न्यूरोफाइब्रोमैटोसिस से उनका संबंध। साहित्य की समीक्षा और सात मामलों की रिपोर्ट। सर्जन न्यूरोल। 1989 अगस्त, 32 (2): 131-6.
- इवांस डीजीआर, बिर्च जेएम, रैम्सडेन आर। टाइप 2 न्यूरोफाइब्रोमैटोसिस की बाल चिकित्सा प्रस्तुति। आर्क डिस चाइल्ड 1998; 81: 496-499।
- इवांस डीजीआर, ह्यूसन एसएम, डोनाई डी, नेरी डब्ल्यू, ब्लेयर वी, न्यूटन वी, हैरिस आर। टाइप 2 न्यूरोफाइब्रोमैटोसिस का नैदानिक अध्ययन। क्यू जे मेड 1992; 84: 603-618।
- इवांस डीजीआर, ह्यूसन एसएम, डोनाई डी, नेरी डब्ल्यू, ब्लेयर वी, न्यूटन वी, स्ट्रैचन टी, हैरिस आर। यूनाइटेड किंगडम में टाइप 2 न्यूरोफाइब्रोमैटोसिस का आनुवंशिक अध्ययन। द्वितीय. आनुवंशिक परामर्श के लिए दिशानिर्देश। जे मेड जेनेट 1992; 29: 847-852।
- इवांस डीजीआर, ह्यूसन एसएम, डोनाई डी, नेरी डब्ल्यू, ब्लेयर वी, टीयर डी, न्यूटन वी, स्ट्रैचन टी, रैम्सडेन आर, हैरिस आर। यूनाइटेड किंगडम में टाइप 2 न्यूरोफाइब्रोमैटोसिस का आनुवंशिक अध्ययन। I. प्रसार, उत्परिवर्तन दर, फिटनेस, और गंभीरता पर मातृ संचरण प्रभाव की पुष्टि। जे मेड जेनेट 1992; 29: 841-846।
- इवांस डीजीआर, ह्यूसन एसएम, पॉन्डर एम, स्ट्रैचन टी, हार्डिंग ए। स्पाइनल और त्वचीय स्च्वानोमैटोसिस टाइप 2 न्यूरोफाइब्रोमैटोसिस का एक भिन्न रूप है। जे न्यूरोल न्यूरोसर्ज मनश्चिकित्सा १९९७; ६२: ३६१-३६६।
- इवांस डीजीआर, रैम्सडेन आर, ह्यूसन एसएम, हैरिस आर, लाइ आर, किंग टीटी। टाइप 2 न्यूरोफाइब्रोमैटोसिस: सुपररीजनल केयर की आवश्यकता? जे लेरिंगोल ओटोल 1993; 107: 401-406।
- इवांस डीजीआर, वालेस ए, ट्रूमैन एल, वू सीएल, रैम्सडेन आरटी, स्ट्रैचन टी। शास्त्रीय न्यूरोफिब्रोमैटोसिस टाइप 2 में मोज़ेकवाद: ट्यूमर प्रवण सिंड्रोम में छिटपुट रोग के लिए एक सामान्य तंत्र? एम जे हम जेनेट 1998; 63: 727-736।
- इवांस जीआर, सी वाटसन, ए किंग, ए जे वालेस और एम ई बेसर। मल्टीपल मेनिंगियोमास: बच्चों और वयस्कों में NF2 जीन की अंतर भागीदारी। जे. मेड. जेनेट। २००५; ४२; ४५-४८.
- फीलिंग ए, वार्ड ई। ध्वनिक ट्यूमर का पारिवारिक रूप। बीएमजे 1920; 10: 496-497।
- फुची एमजे, बुकमैन सीए, ब्रैकमैन डीई, बर्लिनर केआई। ध्वनिक ट्यूमर वृद्धि: उपचार विकल्पों के लिए निहितार्थ। एम जे ओटोल 1999; 20: 495-499।
- गैरेथ आर इवांसा, एम सैनीओब, माइकल ई बसरक। न्यूरोफाइब्रोमैटोसिस टाइप 2. जे मेड जेनेट 2000; 37: 897-904
- गॉटफ्राइड ओरेन एन।, विस्कोचिल डेविड एच।, फुल्ट्स डैनियल डब्ल्यू।, कैनवेल विलियम टी। न्यूरोफिब्रोमास और सर्जिकल निहितार्थ के आणविक, आनुवंशिक और सेलुलर रोगजनन। न्यूरोसर्जरी 58: 1-16, 2006।
- ग्रोनहोम एम। सैनियो एम। झाओ एफ। हिस्का एल। वाहेरी ए। कारपेन ओ। न्यूरोफाइब्रोमैटोसिस 2 ट्यूमर सप्रेसर प्रोटीन मर्लिन और ईआरएम प्रोटीन एज़्रिन का होमोटाइपिक और हेटेरोटाइपिक इंटरैक्शन। जे सेल साइंस 1999; 112: 895-904।
- गुटमैन डीएच। जिओर्डानो एमजे। फिशबैक ए.एस. गुहा ए। छिटपुट मेनिंगिओमास, एपेंडिमोमास और श्वानोमास में मर्लिन अभिव्यक्ति का नुकसान। न्यूरोलॉजी 1997; 49: 267-270।
- हार्टमैन सी, सीबर्न्स जे, गेहलहार सी, साइमन एम, पॉलस डब्ल्यू, वॉन डीमलिंग ए। एनएफ 2 म्यूटेशन इन सेक्रेटरी एंड अदर रेयर वेरिएंट ऑफ मेनिंगियोमास। ब्रेन पैथोल। २००६ जनवरी; १६ (१): १५-९
- हेसेलेगर जी, हॉलैंड ईसी: मस्तिष्क ट्यूमर के आणविक आनुवंशिकी को समझने के लिए चूहों का उपयोग करना। न्यूरोसर्जरी 53: 685-695, 2003।
- हुइन्ह डीपी, मौटनर वी, बेसर एमई, स्टावरौ डी, पुलस्ट एसएम। वेस्टिबुलर श्वानोमास, एपेंडिमोमास और मेनिंगिओमास में श्वाननोमिन और न्यूरोफिब्रोमिन का इम्यूनोहिस्टोकेमिकल डिटेक्शन। जे न्यूरोपैथोल Expक्स्प न्यूरोल १९९७; ५६: ३८२-३९०।
- कैसर-कुफ़र एमआई, फ़्रीडलिन वी, डेटाइल्स एमबी, एल्ड्रिज आर। न्यूरोफाइब्रोमैटोसिस टाइप 2 के रोगियों में द्विपक्षीय ध्वनिक न्यूरोमा के साथ पोस्टीरियर कैप्सुलर लेंस अपारदर्शिता का संघ। आर्क ओफ्थाल्मोल 1989; 107: 541-544।
- किम डीजी, पैक एसएच, ची जेजी, चुन वाईके, हान डीएच। NF-2 वाले रोगी में श्वानोमा और मेनिंगियोमा घटकों का मिश्रित ट्यूमर। एक्टा न्यूरोचिर (वीन)। १९९७; १३९ (११): १०६१-४
- कुमार आरए, बेसर एमई, इवांस डीजीआर, वालेस ए, मौटनर वीएफ, क्लूवे एल, रूलेउ जी, जो एच, फ्रीडमैन जेएम। न्यूरोफाइब्रोमैटोसिस 2 (एनएफ 2) में नैदानिक अभिव्यक्तियों का इंट्राफैमिलियल सहसंबंध। एम जे हम जेनेट 1999; 65 (सप्लीमेंट 4): ए155।
- मार्तुजा आरएल, ओजेमैन आरजी। द्विपक्षीय ध्वनिक न्यूरोमा: नैदानिक पहलू, रोगजनन और उपचार। न्यूरोसर्जरी 1982; 10: 1-12।
- माउटनर वीएफ, लिंडेनौ एम, बेसर एमई, हाज़िम डब्ल्यू, तातागिबा एम, हासे डब्ल्यू, सामी एम, वाइस आर, पुलस्ट एसएम। न्यूरोफाइब्रोमैटोसिस टाइप 2 के रोगियों में स्पाइनल ट्यूमर: आवृत्ति, बहुलता और विविधता का एमआर इमेजिंग अध्ययन (एजेआर 1996 में प्रकाशित इरेटम प्रकट होता है; 166: 1231)। एजेआर १९९५; १६५: ९५१-९५५।
- माउटनर वीएफ, लिंडेनौ एम, बेसर एमई, क्लुवे एल, गॉट्सचॉक जे। न्यूरोफाइब्रोमैटोसिस में त्वचा की असामान्यताएं 2. आर्क डर्माटोल 1997; 133: 1539-1543।
- माउटनर वीएफ, लिंडेनौ एम, बेसर एमई, टाटागिबा एम, हासे डब्ल्यू, सामी एम, वाइस आर, पुलस्ट एसएम। न्यूरोफिब्रोमैटोसिस के न्यूरोइमेजिंग और नैदानिक स्पेक्ट्रम 2. न्यूरोसर्जरी 1996; 38: 880-885।
- माउटनर वीएफ, टाटागिबा एम, गुथॉफ आर, सामी एम, पुलस्ट एसएम। बाल आयु वर्ग में न्यूरोफाइब्रोमैटोसिस 2। न्यूरोसर्जरी 1993; 33: 92-96।
- न्यूरोफाइब्रोमैटोसिस पर स्वास्थ्य सहमति विकास सम्मेलन वक्तव्य के राष्ट्रीय संस्थान। आर्क न्यूरोल 1987; 45: 575-579।
- ओटिबी एम, रुतका जेटी। बच्चों में न्यूरोफाइब्रोमैटोसिस टाइप I के न्यूरोसर्जिकल निहितार्थ। न्यूरोसर्ज फोकस। २००६ जनवरी १५; २० (१)
- पैरी डीएम, एल्ड्रिज आर, कैसर-कुफ़र एमआई, बौज़स ईए, पिकस ए, पेट्रोनास एन। न्यूरोफाइब्रोमैटोसिस 2 (एनएफ 2): 63 प्रभावित व्यक्तियों की नैदानिक विशेषताएं और विषमता के लिए नैदानिक साक्ष्य। एम जे मेड जेनेट 1994; 52: 450-451।
- रैगेल बीटी, जेन्सेन आरएल। मेनिंगियोमा के आणविक आनुवंशिकी। न्यूरोसर्ज फोकस। २००५ नवम्बर १५; १९ (५)
- रैग एनके, बेसर एमई, क्लेन जे, नेचिपोरुक ए, सैंज जे, पुलस्ट एसएम, रिकार्डी वीएम। न्यूरोफाइब्रोमैटोसिस में ओकुलर असामान्यताएं 2. एम जे ओफ्थाल्मोल 1995; 120: 634-641।
- रटलेज एमएच, रूलेउ जीए। तंत्रिका तंत्र के ट्यूमर के विकास में न्यूरोफाइब्रोमैटोसिस टाइप 2 जीन की भूमिका। न्यूरोसर्ज फोकस। २००५नवंबर; 19 (5).
- स्लेटरी डब्ल्यूएच, ब्रैकमैन डीई, हिट्सेलबर्गर डब्ल्यू। न्यूरोफाइब्रोमैटोसिस टाइप 2 में हियरिंग प्रिजर्वेशन। एम जे ओटोल 1998; 19: 638-643।
- थॉमस पीके, किंग आरएचएम, चियांग टीआर, स्कारविल्ली एफ, शर्मा एके, डाउनी एडब्ल्यू। न्यूरोफाइब्रोमैटस न्यूरोपैथी। स्नायु तंत्रिका 1990; 13: 93-101।
- टोमिता टी, राडकोव्स्की एमए, गोंजालेज-क्रूसी एफ, ज़ापाराकस जेड, फ्लैनरी ए। एक बच्चे में एकाधिक मेनिंगियोमा। सर्जन न्यूरोल। १९८८ फ़रवरी, २९ (२): १३१-६.
- सुकिता एस, योनमुरा एस। कॉर्टिकल एक्टिन संगठन: ईआरएम (एज़्रिन / रेडिक्सिन / मोएसिन) प्रोटीन से सबक। जे बायोल केमिस्ट्री 1999; 274: 34507-34510।
- टर्गुट एम, पलाओग्लू एस, ओज़्कन ओई। न्यूरोफाइब्रोमैटोसिस 2 के न्यूरोसर्जिकल पहलू: निदान और प्रबंधन। न्यूरोसर्जन रेव. 1998; 21 (1): 23-30।
- जांग के.डी. मानव मेनिंगियोमा पर साइटोलॉजिकल और साइटोजेनेटिक अध्ययन। कैंसर जेनेट साइटोजेनेट 1982; 6: 249-274।
- Zucman-रॉसी जम्मू, Legoix पी, Sarkissian HD, Cheret जी, सोर एफ, Berardi ए, Cazes एल, गिरौड एस, Ollagnon ई, Lenoir जी, न्यूरोफाइब्रोमैटॉसिस टाइप 2 रोगियों में थॉमस जी NF2 जीन। हम मोल जेनेट 1998; 7: 2095-2101।